Durante décadas hemos sabido que el ejercicio protege el cerebro del envejecimiento, pero sin entender bien por qué. Un estudio publicado en Cell en febrero de 2026 por investigadores de la Universidad de California en San Francisco (UCSF) propone un mecanismo concreto: el hígado, cuando recibe la señal del ejercicio, libera una enzima llamada GPLD1 que viaja por la sangre hasta los vasos cerebrales y elimina una proteína acumulada con la edad —la TNAP— que hace que la barrera hematoencefálica se vuelva porosa. En ratones viejos tratados con GPLD1, la barrera se restauró, la inflamación cerebral bajó y la memoria mejoró. Es un hallazgo mecanístico sólido e importante. Sin embargo, todo el trabajo experimental se ha realizado en modelos animales. No hay ensayos clínicos en humanos. El entusiasmo está justificado, pero la distancia entre un resultado en ratones y un tratamiento validado en personas es enorme. Por ahora, el ejercicio regular sigue siendo la única intervención con evidencia real en humanos.
¿Y si el hígado fuese el intermediario que siempre buscamos?
Hay datos epidemiológicos sólidos, consolidados durante décadas, que muestran que las personas físicamente activas mantienen mejor función cognitiva en la vejez y tienen menos riesgo de demencia. El problema ha sido siempre el mismo: sabemos el qué, pero no el cómo. ¿Qué ocurre exactamente entre el momento en que una persona sale a caminar y el momento en que su cerebro sale beneficiado?
La respuesta intuitiva señalaba al músculo. O a la mejora circulatoria. O al BDNF, ese factor neurotrófico que el ejercicio eleva y que se asocia a la neurogénesis. Pero un estudio publicado el 18 de febrero de 2026 en Cell —una de las revistas científicas de mayor impacto del mundo— propone un actor inesperado: el hígado.
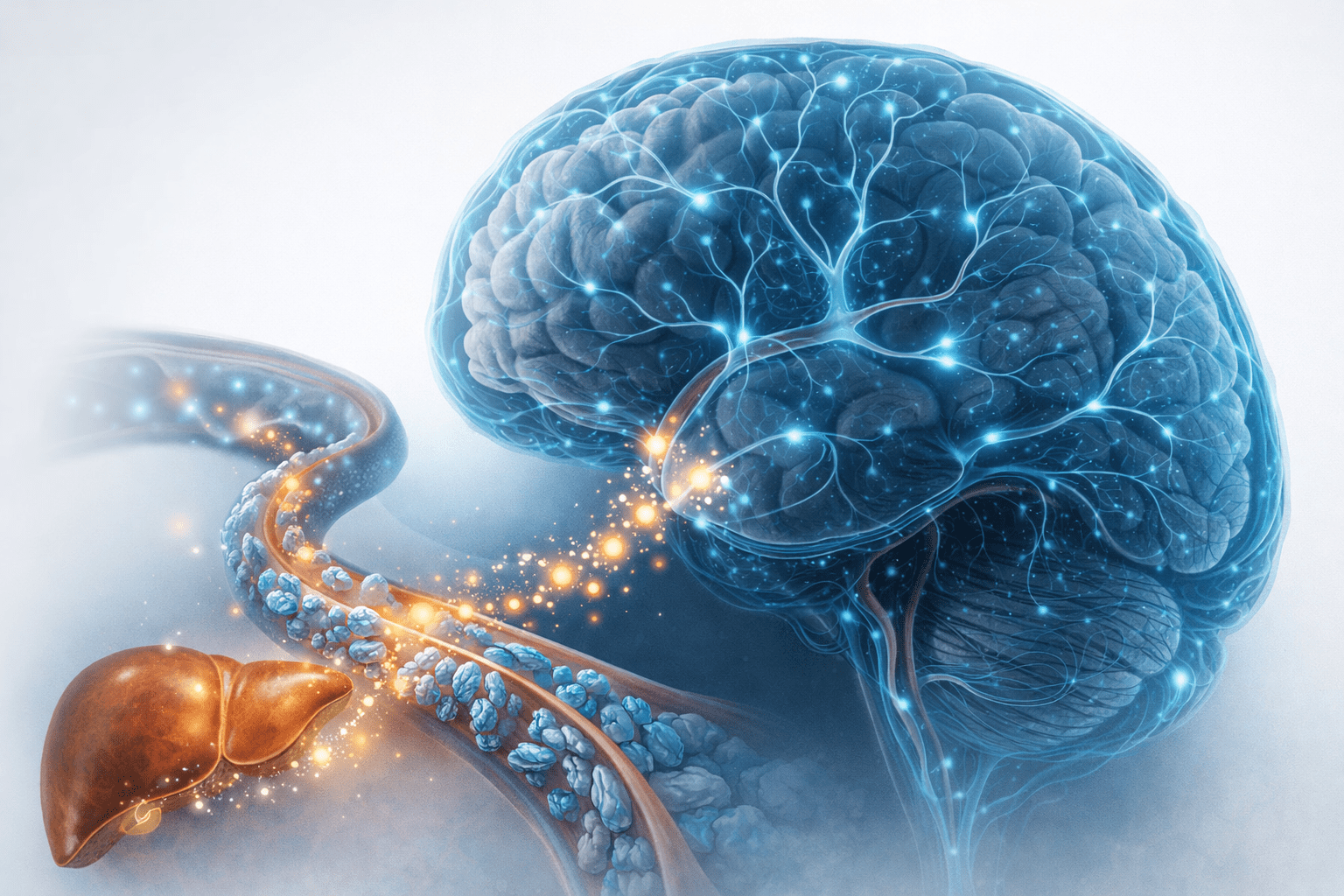
La investigación, liderada por Saul Villeda en el UCSF Bakar Aging Research Institute, identifica un circuito que nadie había descrito con esta precisión: el ejercicio instruye al hígado para que fabrique una enzima; esa enzima viaja por la sangre; llega a los vasos que rodean el cerebro; allí elimina una proteína que, acumulada con los años, convierte la barrera hematoencefálica en un tamiz con fugas. El resultado, al menos en ratones viejos, es un cerebro que funciona mejor.
Es un hallazgo elegante. Y merece ser analizado con la atención —y el escepticismo— que requiere.
Qué es la barrera hematoencefálica y por qué importa que no tenga fugas
La barrera hematoencefálica (BHE) es una estructura formada por células endoteliales muy especializadas que tapizan los capilares cerebrales. Su función es crear una frontera selectiva entre la sangre circulante —con sus toxinas, patógenos y moléculas diversas— y el delicado tejido neuronal. Lo que entra al cerebro debe pasar por un control estricto.
Con la edad, esta frontera pierde integridad. Las uniones entre células endoteliales se aflojan, y la barrera se vuelve permeable a sustancias que no deberían cruzarla. El fenómeno se conoce informalmente como leaky blood-brain barrier o, con menos eufemismos, “cerebro con fugas”. Cuando sustancias inflamatorias o proteínas dañinas se cuelan, el cerebro responde con inflamación crónica de bajo grado, un estado que se ha asociado con el deterioro cognitivo del envejecimiento y con enfermedades neurodegenerativas como el Alzheimer.
Un estudio observacional con personas mayores ya había detectado una correlación entre mayor permeabilidad de la barrera y peores puntuaciones en pruebas cognitivas. No era una sorpresa conceptual, pero confirmaba que el sellado de esa frontera importa. La pregunta pendiente era qué provoca el sellado y cómo restaurarlo cuando falla.
El mecanismo: ejercicio → hígado → GPLD1 → TNAP → barrera más estanca
El grupo de Villeda lleva años trabajando con un modelo experimental elegante: el plasma de ratones jóvenes, transfundido a ratones viejos, mejora la función cognitiva de estos. Eso sugería que la sangre joven contiene factores protectores que la sangre vieja ha perdido. Hace seis años, el mismo equipo identificó que el ejercicio elevaba en el hígado una enzima llamada GPLD1 (glicosylfosfatidilinositol-fosfolipasa D1), y que sus niveles plasmáticos se asociaban a beneficios cognitivos.
El problema era un callejón sin salida aparente: GPLD1 no cruza la barrera hematoencefálica. Si no puede entrar al cerebro, ¿cómo actúa sobre él?
La respuesta que ofrece este estudio es elegante. GPLD1 no necesita entrar al cerebro. Le basta con actuar sobre su exterior, concretamente sobre la superficie de las células endoteliales que forman la barrera. Su función molecular es la de unas tijeras: corta proteínas ancladas a la membrana de las células.
Los investigadores rastrearon sistemáticamente qué proteínas de la superficie endotelial cerebral eran susceptibles de ser cortadas por GPLD1. Entre varias candidatas, solo una resistió: la TNAP (fosfatasa alcalina inespecífica de tejido). Y aquí el hallazgo se vuelve narrativamente coherente:
- En ratones jóvenes, la TNAP está presente en niveles bajos en los vasos cerebrales.
- Con la edad, la TNAP se acumula progresivamente en esas células endoteliales.
- Cuanta más TNAP, más porosa se vuelve la barrera.
- El ejercicio induce la producción hepática de GPLD1.
- La GPLD1 circula en sangre, llega a los vasos cerebrales y recorta la TNAP acumulada.
- La barrera recupera su integridad.
Para verificar la causalidad, el equipo utilizó ingeniería genética en ambas direcciones. Ratones jóvenes con TNAP artificialmente elevada en los vasos cerebrales desarrollaron problemas de memoria similares a los de animales viejos. Ratones equivalentes a personas de 70 años, a los que se redujo genéticamente la TNAP, vieron reducirse la permeabilidad de la barrera, bajar la inflamación cerebral y mejorar su rendimiento en pruebas de memoria. El efecto era bidireccional y coherente.
Además, cuando se administró directamente GPLD1 a ratones viejos —mediante instrucciones genéticas para que su hígado produjera más enzima, simulando el efecto del ejercicio—, los resultados fueron similares: barrera más estanca, menos inflamación, mejor memoria. Y los perfiles de expresión génica en las células endoteliales envejecidas se desplazaron hacia patrones más juveniles.
El nexo con el Alzheimer
El equipo fue más allá del envejecimiento normal. Utilizó ratones modificados genéticamente para desarrollar placas de beta-amiloide, el sello patológico del Alzheimer. En estos animales, el tratamiento con GPLD1 —o con un inhibidor farmacológico directo de la TNAP llamado SBI-425— redujo la densidad de placas en el hipocampo y mejoró comportamientos indicativos de bienestar. También se analizaron muestras de cerebro humano de personas con Alzheimer confirmado: los vasos cerebrales mostraban niveles elevados de TNAP en comparación con controles. Correlación, no causalidad, pero el patrón es coherente con la hipótesis.
El dato es interesante, pero hay que leerlo con cuidado. Que los cerebros de personas con Alzheimer tengan más TNAP en los vasos no prueba que la TNAP cause Alzheimer, ni que reducirla en humanos tenga los mismos efectos que en ratones modificados. La fisiopatología del Alzheimer en humanos es mucho más compleja, heterogénea y multifactorial que la de cualquier modelo animal disponible.
Lo que la ciencia NO dice (y conviene aclarar)
Este es un estudio mecanístico de alta calidad, publicado en una revista de primer nivel, con un diseño experimental sólido y resultados internamente coherentes. Y, aun así, hay varias cosas que no podemos concluir de él:
El hallazgo está íntegramente en ratones. No hay un solo dato clínico en humanos que demuestre que elevar GPLD1 o reducir TNAP mejore la memoria o proteja frente al Alzheimer en personas reales. La tasa de fracaso en la traslación de resultados de modelos animales a ensayos clínicos en neurología es especialmente alta. Más del 99% de los fármacos que han funcionado en modelos animales de Alzheimer han fracasado en ensayos con humanos. Este contexto no invalida el hallazgo, pero obliga a la cautela.
No sabemos si la GPLD1 es el factor principal del efecto neuroprotector del ejercicio, ni siquiera en ratones. Los autores mismos reconocen que el BDNF, la irisina, el factor plaquetario 4 (PF4) y otros factores sistémicos probablemente contribuyen. El eje hígado-cerebro descrito aquí es un elemento del rompecabezas, posiblemente importante, pero no la imagen completa.
El riesgo de sellar en exceso la barrera. La barrera hematoencefálica no es solo una muralla; también es una vía de salida. El sistema glinfático, activo principalmente durante el sueño, utiliza los espacios perivasculares para eliminar desechos metabólicos del cerebro, incluido el beta-amiloide. Una barrera excesivamente rígida podría, paradójicamente, dificultar esa limpieza nocturna. Los autores reconocen este potencial conflicto, y es una pregunta que cualquier futuro fármaco basado en este mecanismo deberá responder antes de llegar a clínica.
Las noticias del “medicamento que simula el ejercicio” circulan desde la publicación del estudio con un entusiasmo que supera ampliamente lo que los datos justifican. El SBI-425 ha funcionado en ratones. No ha sido probado en personas. El camino desde un resultado animal hasta un fármaco aprobado es largo, costoso y estadísticamente improbable.
Qué significa esto para la práctica
Para cualquier persona que se pregunte qué hace con este hallazgo en su vida cotidiana, la respuesta es decepcionantemente sencilla: nada nuevo, por ahora. El ejercicio regular sigue siendo la única intervención con evidencia robusta y replicada en humanos para reducir el riesgo de deterioro cognitivo. Esta investigación añade un mecanismo molecular plausible que podría explicar parcialmente ese beneficio. Eso es valioso científicamente. Pero no cambia la prescripción.
Lo que sí cambia es la perspectiva conceptual. El cerebro ya no puede estudiarse como un órgano aislado que solo responde a lo que ocurre dentro de la caja craneal. La señal parte del músculo en contracción, el hígado la traduce, y la barrera vascular la ejecuta. El cuerpo habla al cerebro a través de un idioma que apenas estamos empezando a descifrar.
Para quienes no pueden hacer ejercicio —por enfermedad, discapacidad o edad avanzada—, la vía farmacológica sobre TNAP abre una posibilidad teórica de replicar parte de ese beneficio. Es una promesa razonable. Pero todavía es solo una promesa.
Conclusión
El estudio de Bieri, Villeda y colaboradores es ciencia de calidad: mecanismo claro, diseño experimental riguroso, publicado con revisión por pares en Cell. Identifica un eje hígado-cerebro mediado por GPLD1 y TNAP que explica, en ratones, cómo el ejercicio puede restaurar la integridad de la barrera hematoencefálica y mejorar la función cognitiva en el envejecimiento. La coherencia del modelo, con sus validaciones en ambas direcciones, es metodológicamente convincente.
Pero estamos en fase preclínica. No hay evidencia de eficacia en humanos, ni de seguridad a largo plazo, ni de que este mecanismo tenga el mismo peso en la biología humana que en la murina. Los titulares sobre “el medicamento que imita el ejercicio” o “la clave para prevenir el Alzheimer” van, como de costumbre, muy por delante de lo que el paper realmente demuestra.
Lo que sí podemos decir con seguridad: el ejercicio aeróbico regular tiene evidencia sólida en humanos para reducir el riesgo de demencia. Si existe una dosis mínima eficaz reconocida, estaríamos hablando de al menos 150 minutos semanales de actividad moderada, conforme a las recomendaciones de la OMS. Ese es el tratamiento disponible hoy. Todo lo demás es ciencia en curso, y bienvenida sea.
Bibliografía
- Bieri G, Pratt KJB, Fuseya Y, et al. “Liver exerkine reverses aging- and Alzheimer’s-related memory loss via vasculature.” Cell. 2026. DOI: 10.1016/j.cell.2026.01.024
- UCSF News. “Scientists Find a Mechanism for How Exercise Protects the Brain.” 17 febrero 2026. ucsf.edu
- Montagne A, et al. “Blood-brain barrier breakdown in the aging human hippocampus.” Neuron. 2015;85(2):296-302. PubMed
- Kivipelto M, et al. “Lifestyle interventions to prevent cognitive impairment, dementia and Alzheimer disease.” Nature Reviews Neurology. 2018;14(11):653-666. PubMed
- Livingston G, et al. “Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission.” The Lancet. 2024;404(10452):572-628. PubMed
- World Health Organization. “Global action plan on physical activity 2018–2030.” Geneva: WHO; 2018. who.int








Average Rating